O cloreto de prata (AgCl) consiste em um importante sal da química inorgânica, e apresenta em sua estrutura um cátion, derivado do elemento químico prata, e um ânion, derivado do elemento químico cloro, monovalentes. Existe como um sólido branco cristalino. Sua molécula é formada a partir de uma forte ligação de natureza iônica,
o que faz com que o sal seja conhecido no laboratório por sua
insolubilidade em água e fotossensibilidade quando sólido. Ainda com
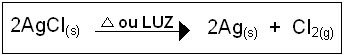
base em seu comportamento físico, produz prata metálica (Ag) e libera
gás cloro (Cl2) quando aquecido ou sob iluminação, de acordo com a equação abaixo:
O AgCl possui diversas aplicações, sendo que atualmente “é utilizado na confecção de papel
fotográfico, visto que reage com fótons para formar imagens, seu
eletrodo é muito utilizado na eletroquímica, tem sido usado como
antídoto para envenenamento por mercúrio (Hg) e na fabricação de vidros
coloridos, nas cores amarela, âmbar e marrom. O AgCl possui também ação
antimicrobiana, sendo por isso também utilizado em materiais cirúrgicos e
materiais para tratamento de feridas.”1
Laboratorialmente, a síntese do cloreto de prata a partir do cloreto de sódio (NaCl) e nitrato de prata (AgNO3) presta-se muito bem didaticamente para a compreensão de uma reação química, que é um sistema
no qual há alteração da natureza da matéria entre os envolvidos. Nesta
reação, na qual os dois sais utilizados são comumente encontrados em um
laboratório de química, parte-se de duas soluções verdadeiras, visto que
ambos são hidrossolúveis. Entretanto, quando em contato em sua forma
aquosa, tais sais irão formar um composto químico de natureza diferente,
de baixíssima hidrossolubilidade, turvando completamente o meio de
reação, em um aspecto muito diferente do inicial.
Partindo-se de 1g de AgNO3, de modo que a estequiometria
da reação seja estabelecida, será necessária uma massa de NaCl de
0,34g. Ambas devem ser inicialmente hidrossolubilizadas, em qualquer
concentração, para que a reação ocorra em meio aquoso. Dessa forma,
teremos um precipitado de AgCl, o qual pode então ser filtrado e ter sua
massa medida, após evaporação da água residual. De acordo com a equação
abaixo, pode-se notar que sua massa teórica esperada é 0,84g, a qual,
devido à impureza dos reagentes e a outros fatores, experimentalmente
raramente é obtida, podendo-se também calcular na sequência o rendimento da reação.
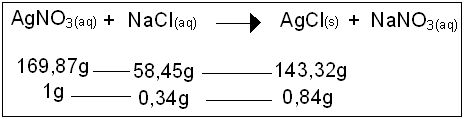
Na primeira linha de valores é mostrado os pesos moleculares de cada
um dos sais, e na segunda, a massa necessária de NaCl e a massa esperada
de AgCl, apartir de 1g de AgNO3. Laboratorialmente, logo
após a reação deve-se proceder pelo armazenamento do sólido produzido em
frasco âmbar devido a sua alta fotossensibilidade, a qual evidencia-se
pelo rápido escurecimento, devido a liberação de Cl2 e conseqüente formação de prata metálica.

Nenhum comentário:
Postar um comentário